Alzheimers sykdom, det vanligste tilfellet blant eldre, har plaget folk flest.
En av utfordringene i behandlingen av Alzheimers sykdom er at tilførselen av terapeutiske legemidler til hjernevev er begrenset av blod-hjerne-barrieren. Studien fant at MR-veiledet lavintensitetsfokusert ultralyd reversibelt kan åpne blod-hjerne-barrieren hos pasienter med Alzheimers sykdom eller andre nevrologiske lidelser, inkludert Parkinsons sykdom, hjernesvulster og amyotrofisk lateral sklerose.
En nylig liten konseptstudie ved Rockefeller Institute for Neuroscience ved West Virginia University viste at pasienter med Alzheimers sykdom som fikk aducanumab-infusjon i kombinasjon med fokusert ultralyd midlertidig åpnet blod-hjerne-barrieren, reduserte belastningen på amyloid beta (Aβ) i hjernen betydelig på studiesiden. Forskningen kan åpne nye dører for behandlinger for hjernesykdommer.
Blod-hjerne-barrieren beskytter hjernen mot skadelige stoffer samtidig som den lar essensielle næringsstoffer passere. Men blod-hjerne-barrieren forhindrer også tilførsel av terapeutiske legemidler til hjernen, en utfordring som er spesielt akutt ved behandling av Alzheimers sykdom. Etter hvert som verden eldes, øker antallet mennesker med Alzheimers sykdom år for år, og behandlingsmulighetene er begrensede, noe som legger en tung belastning på helsevesenet. Aducanumab er et amyloid beta (Aβ)-bindende monoklonalt antistoff som er godkjent av US Food and Drug Administration (FDA) for behandling av Alzheimers sykdom, men penetrasjonen av blod-hjerne-barrieren er begrenset.
Fokusert ultralyd produserer mekaniske bølger som induserer svingninger mellom kompresjon og fortynning. Når boblene injiseres i blodet og eksponeres for ultralydfeltet, komprimeres og utvides de mer enn det omkringliggende vevet og blodet. Disse svingningene skaper mekanisk stress på blodåreveggen, noe som fører til at de tette forbindelsene mellom endotelcellene strekkes og åpnes (figur nedenfor). Som et resultat kompromitteres integriteten til blod-hjerne-barrieren, slik at molekyler kan diffundere inn i hjernen. Blod-hjerne-barrieren leges av seg selv på omtrent seks timer.
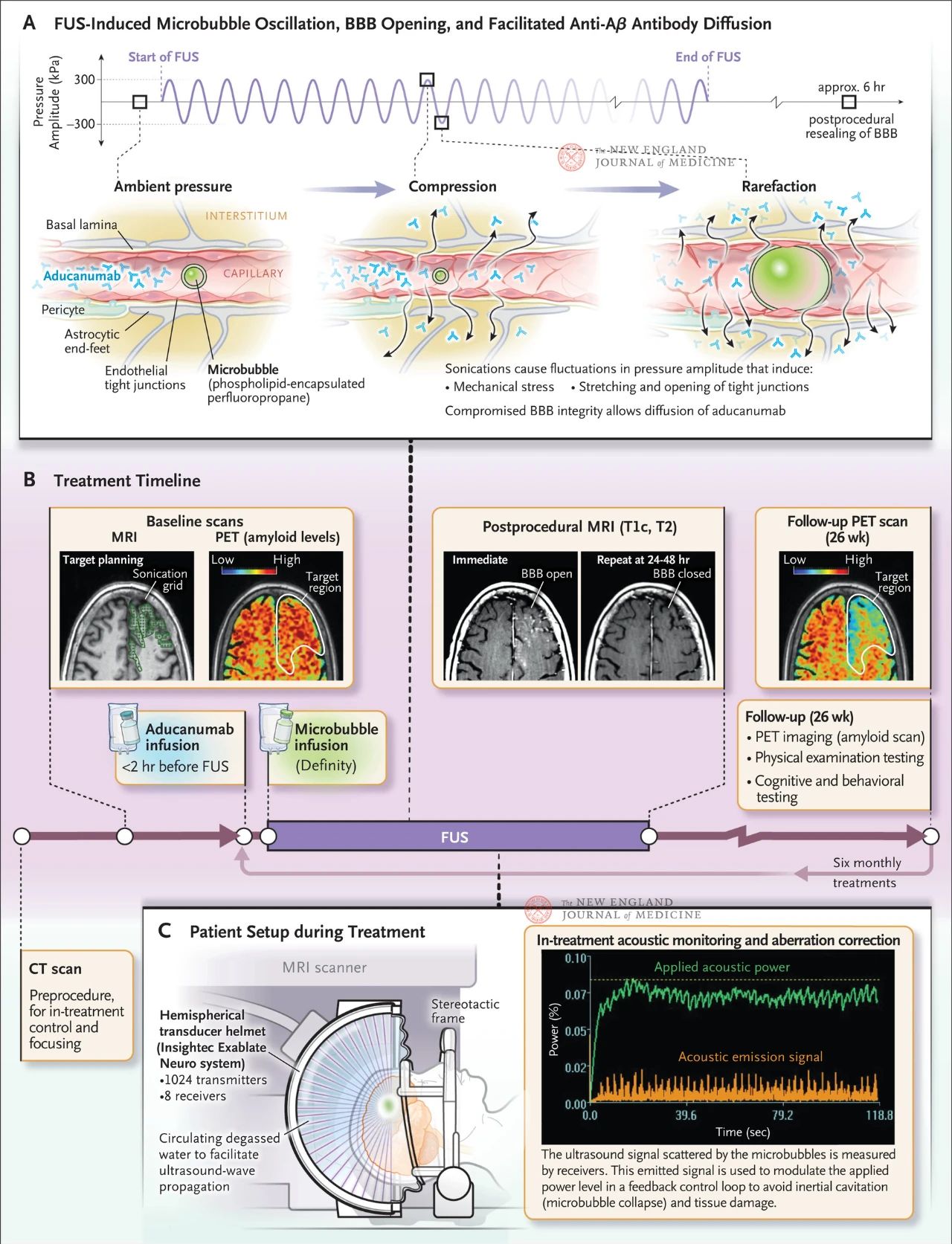
Figuren viser effekten av retningsbestemt ultralyd på kapillærvegger når det finnes mikrometerstore bobler i blodårene. På grunn av gassenes høye kompressibilitet trekker boblene seg sammen og utvider seg mer enn det omkringliggende vevet, noe som forårsaker mekanisk stress på endotelcellene. Denne prosessen fører til at tette forbindelser åpnes og kan også føre til at astrocyttender faller av blodåreveggen, noe som kompromitterer integriteten til blod-hjerne-barrieren og fremmer antistoffdiffusjon. I tillegg forbedret endotelceller eksponert for fokusert ultralyd sin aktive vakuolære transportaktivitet og undertrykte efflukspumpefunksjonen, og reduserte dermed hjernens clearance av antistoffer. Figur B viser behandlingsplanen, som inkluderer computertomografi (CT) og magnetisk resonansavbildning (MR) for å utvikle ultralydbehandlingsplanen, 18F-flubitaban positronemisjonstomografi (PET) ved baseline, antistoffinfusjon før fokusert ultralydbehandling og mikrovesikulær infusjon under behandling, og akustisk overvåking av de mikrovesikulære sprednings-ultralydsignalene som brukes til å kontrollere behandlingen. Bildene som ble tatt etter fokusert ultralydbehandling inkluderte T1-vektet kontrastforsterket MR, som viste at blod-hjerne-barrieren var åpen i det ultralydbehandlede området. Bilder av det samme området etter 24 til 48 timer med fokusert ultralydbehandling viste fullstendig tilheling av blod-hjerne-barrieren. En 18F-flubitaban PET-skanning under oppfølging hos en av pasientene 26 uker senere viste reduserte Aβ-nivåer i hjernen etter behandling. Figur C viser det MR-veiledede fokuserte ultralydoppsettet under behandlingen. Den halvkuleformede transduserhjelmen inneholder mer enn 1000 ultralydkilder som konvergerer til et enkelt fokuspunkt i hjernen ved hjelp av sanntidsveiledning fra MR.
I 2001 ble det i dyrestudier først vist at fokusert ultralyd induserer åpning av blod-hjerne-barrieren, og påfølgende prekliniske studier har vist at fokusert ultralyd kan forbedre medikamenttilførsel og effekt. Siden den gang har det blitt funnet at fokusert ultralyd trygt kan åpne blod-hjerne-barrieren hos pasienter med Alzheimers som ikke får medisiner, og kan også levere antistoffer mot hjernemetastaser i brystkreft.
Mikrobobleleveringsprosess
Mikrobobler er et ultralydkontrastmiddel som vanligvis brukes til å observere blodstrøm og blodkar i ultralyddiagnostikk. Under ultralydbehandling ble en fosfolipidbelagt ikke-pyrogen boblesuspensjon av oktafluorpropan injisert intravenøst (figur 1B). Mikroboblene er svært polydisperse, med diametre fra mindre enn 1 μm til mer enn 10 μm. Oktafluorpropan er en stabil gass som ikke metaboliseres og kan skilles ut gjennom lungene. Lipidskallet som omslutter og stabiliserer boblene er sammensatt av tre naturlige humane lipider som metaboliseres på en lignende måte som endogene fosfolipider.
Generering av fokusert ultralyd
Fokusert ultralyd genereres av en halvkuleformet transduserhjelm som omgir pasientens hode (figur 1C). Hjelmen er utstyrt med 1024 uavhengig kontrollerte ultralydkilder, som er naturlig fokusert i midten av hjernehalvdelen. Disse ultralydkildene drives av sinusformede radiofrekvensspenninger og sender ut ultralydbølger styrt av magnetisk resonansavbildning. Pasienten bruker hjelm, og avgasset vann sirkulerer rundt hodet for å legge til rette for ultralydoverføring. Ultralyden beveger seg gjennom huden og hodeskallen til hjernemålet.
Endringer i skallens tykkelse og tetthet vil påvirke ultralydforplantningen, noe som resulterer i litt ulik tid det tar for ultralyd å nå lesjonen. Denne forvrengningen kan korrigeres ved å innhente høyoppløselige computertomografidata for å få informasjon om skallens form, tykkelse og tetthet. En datasimuleringsmodell kan beregne det kompenserte faseskiftet for hvert drivsignal for å gjenopprette det skarpe fokuset. Ved å kontrollere fasen til RF-signalet kan ultralyden fokuseres elektronisk og plasseres for å dekke store mengder vev uten å bevege ultralydkildematrisen. Plasseringen av målvevet bestemmes ved magnetisk resonansavbildning av hodet mens man bruker hjelm. Målvolumet fylles med et tredimensjonalt rutenett av ultralydforankringspunkter, som sender ut ultralydbølger ved hvert forankringspunkt i 5–10 ms, gjentatt hvert 3. sekund. Ultralydeffekten økes gradvis til ønsket boblespredningssignal oppdages, og holdes deretter i 120 sekunder. Denne prosessen gjentas på andre nett til målvolumet er fullstendig dekket.
Å åpne blod-hjerne-barrieren krever at amplituden til lydbølgene overstiger en viss terskel. Utover denne terskel øker barrierens permeabilitet med økende trykkamplitude inntil vevsskade oppstår, manifestert som erytrocytt-eksosmose, blødning, apoptose og nekrose, som alle ofte er forbundet med boblekollaps (kalt treghetskavitasjon). Terskelen avhenger av mikroboblestørrelsen og skallmaterialet. Ved å oppdage og tolke ultralydsignalene spredt av mikroboblene, kan eksponeringen holdes innenfor et trygt område.
Etter ultralydbehandling ble T1-vektet MR med kontrastmiddel brukt for å avgjøre om blod-hjerne-barrieren var åpen på målstedet, og T2-vektede bilder ble brukt for å bekrefte om det forekom ekstravasasjon eller blødning. Disse observasjonene gir veiledning for justering av annen behandling, om nødvendig.
Evaluering og utsikter til terapeutisk effekt
Forskerne kvantifiserte effekten av behandlingen på hjernens Aβ-belastning ved å sammenligne 18F-flubitaban positronemisjonstomografi før og etter behandling for å vurdere forskjellen i Aβ-volum mellom det behandlede området og et lignende område på motsatt side. Tidligere forskning fra samme team har vist at det å fokusere ultralyd kan redusere Aβ-nivåene noe. Reduksjonen som ble observert i denne studien var enda større enn i tidligere studier.
I fremtiden vil det være avgjørende å utvide behandlingen til begge sider av hjernen for å evaluere dens effektivitet i å forsinke sykdomsprogresjon. I tillegg er det behov for mer forskning for å bestemme langsiktig sikkerhet og effekt, og kostnadseffektive terapeutiske apparater som ikke er avhengige av online MR-veiledning må utvikles for bredere tilgjengelighet. Funnene har likevel skapt optimisme om at behandlingen og legemidlene som fjerner Aβ til slutt kan bremse Alzheimers progresjon.
Publisert: 06.01.2024